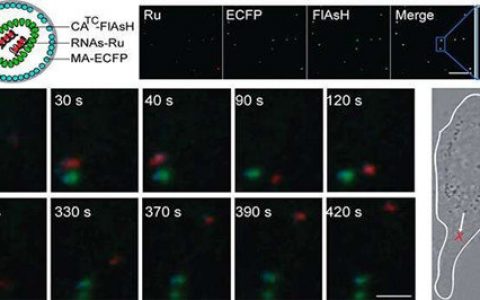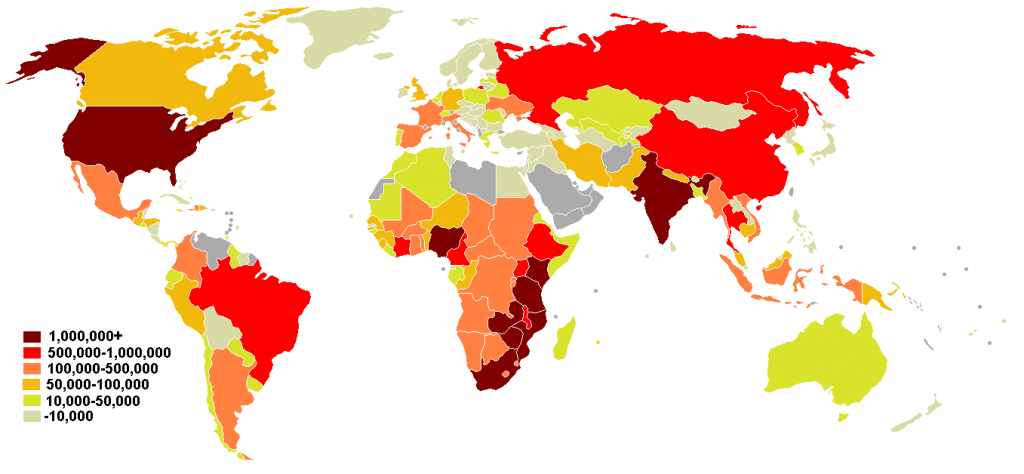
由香港大学(港大)李嘉诚医学院微生物学系爱滋病研究所领导的研究团队,利用基因工程技术,研制出一种新型的串联双价广谱中和抗体(bi-specific bNAb),可有效抑制所有测试过的爱滋病病毒株,并促进清除人源化小鼠体内的潜伏感染细胞。这项研究成果已在最新一期《临床研究杂志》发表。
爱滋病(AIDS)是目前无法治愈的疾病。在全世界,爱滋病病毒(HIV)已经导致约4,000万人死亡,目前仍有约3,690万人携带着爱滋病病毒生活。为遏止爱滋病的全球大流行,研究出有效的爱滋病疫苗或治愈疗法十分重要。然而,HIV的高突变率和抗病毒药物无法清除的潜伏库,仍然是两大科学挑战。因为在人体内极难利用合适的抗原诱导出具有抑制各种爱滋病变异病毒的广谱中和抗体(bNAb),利用已发现的bNAbs进行被动免疫,就成为爱滋病预防和免疫治疗的实用方法。
科学家们通过体内和体外实验,已经针对多种bNAbs及它们组合的有效性、广谱性和晶体结构进行了研究。然而,许多HIV毒株对这些bNAbs 固有耐药,导致基于单一bNAb治疗方案失败。为进一步优化bNAb的有效性和广谱性,研发可以阻止HIV感染细胞两个重要环节的双价中和抗体应运而生,并在动物模型中展现出前景。在本研究之前,还没有学者将串连双价中和抗体用于体内抗HIV做出研究。
港大爱滋病研究所的研究团队发明了一种单基因编码的串连双价广谱中和抗体,并将其命名为「BiIA-SG」,具有「一石二鸟」的效果。BiIA-SG通过结合宿主细胞表面的CD4蛋白,有策略性地伏击HIV,进而保护CD4 + T细胞不被感染。BiIA-SG不仅展示出强大的功效,在体外能有效中和124株不同基因亚型的HIV,而且可以完全保护人源化老鼠免于多种HIV活病毒的感染。此外,基因导入的BiIA-SG可以在人源化老鼠体内持续发挥功效,并且清除已被HIV感染的细胞。因此,此项研究为BiIA-SG作为一种新型抗体药物用于HIV预防和免疫治疗提供了概念验证。
自2009年香港引入抗HIV病毒治疗及预防手段以来,已确诊的HIV感染病例,从2009年的4,443宗已倍增至2017年的9,091宗。目前估计,香港每年用于HIV抗病毒治疗药物的花费超过5亿5千万港元,其中还未包括终身服药的财政负担、药物毒性和耐药病毒等问题。BiIA-SG作为一种普遍适用的抗体药物,其广谱性和有效性有明显改进,将有望真正成为首个「香港制造」,适用于临床治疗HIV的抗体药物。
论文链接:Wu, Xilin, et al. “Tandem bispecific neutralizing antibody eliminates HIV-1 infection in humanized mice.” The Journal of clinical investigation (2018). DOI: 10.1172/JCI96764
本文来自香港大学,本文观点不代表沙鸥科报立场,转载请联系原作者。