据清华大学,该校药学院肖百龙课题组在《神经元》(Neuron)期刊以长文形式在线发表了题为《机械敏感Piezo通道离子通透和机械力传导机制》的研究论文,首次系统报道了Piezo通道如何感知机械力刺激并控制其离子流通的分子作用机制。
机械敏感非选择性阳离子通道是一类能够响应机械力刺激而被快速激活引起钙、钠、钾离子流通的通道蛋白,被认为在触觉/痛觉机械力感受、听觉、血压调节等生理过程中扮演重要角色,科学家也一直致力于寻找其在脊椎动物中的分子组成。直到2010年,美国斯克利普斯研究所(The Scripps Research Institute)的Ardem Patapoutian博士研究组在这一领域取得重大突破,发现了Piezo1和Piezo2两个基因对于机械力门控非选择性阳离子电流的产生至关重要 (Coste et al., Science 2010)。随后研究证实Piezo通道可以作为重要的机械力传感器参与血管发育、触觉感受等基本生物功能。因而,其功能失调极有可能造成心血管、疼痛等方面的疾病。在人体,Piezo1和Piezo2基因编码区上的遗传突变也能够分别引起遗传性干瘪红细胞增多症和远端关节弯曲综合症等遗传疾病,进一步证明它们在人体生理功能的重要性及其与疾病的相关性,以及作为重要药物靶点的前景。
Piezo通道蛋白是一类复杂的膜蛋白家族,与已知离子通道不具备任何序列上的类似性,因而其分子功能并不清楚。肖百龙博士在从事博士后研究期间率先完成对这一复杂大型膜蛋白的重组表达、纯化、理化性质及电生理特性的研究,并首次证明其以多聚体的形式形成哺乳动物中鉴定发现的首类机械敏感阳离子通道的孔道蛋白 (Coste and Xiao et al., Nature, 2012),从而揭开了脊椎动物中这一重要通道分子组成的神秘面纱并确立了Piezo机械力门控离子通道这一全新的离子通道家族。
肖百龙研究员于2013年1月到清华大学药学院组建自己的课题组,并任职清华-北大生命科学联合中心以及清华大学IDG/麦戈文脑科学研究院,致力于对Piezo通道家族的结构功能、生理及病理学意义、及药物筛选与开发研究。利用其课题组在Piezo蛋白的分子生物学、蛋白重组表达及纯化、电生理功能研究的坚实基础,在揭示Piezo通道家族的结构功能关系方面取得系列重要进展。
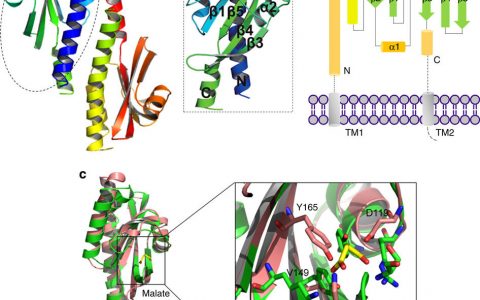
通过与清华大学高宁研究组及杨茂君研究组合作,他所带领的课题组在国际上率先解析重组表达的鼠源全长Piezo蛋白的亚纳米级别分辨率冷冻电镜三维结构。Piezo1同源三聚体整体呈现类似于三叶螺旋桨的架构,远端胞外区呈现扇叶结构,最后一个胞外区正好位于结构中心且呈现帽子样结构,每一个螺旋桨骨架由至少14个明显的跨膜区组成,每个骨架下面还含有一个长的“横梁”支撑上面的跨膜区(图A)。这一整体特殊新颖的结构也暗示了Piezo蛋白家族可能通过胞外的扇叶区去感受机械力进而调控中心成孔区的开放关闭状态。该研究成果于2015年9月21日以长文形式发表在《自然》(Ge et al., Nature 2015)。
Piezo1通道结构的解析为进一步揭示其分子工作机制奠定了重要基础。但是由于其分辨率的限制,Piezo通道的重要功能域定位以及其离子流通和机械力传导的分子机制等问题有待解决。该课题组发表于神经科学领域著名期刊《神经元》的研究长文(Zhao et al., Neuron 2016)聚焦这些关键科学问题,利用生化分析与电生理等功能研究手段,首次报导在序列和结构上高度复杂的Piezo1离子通道以功能区模块化的方式来行使其作为一类精细的机械力门控阳离子通道:其羧基段包含最后两次跨膜区的约350个氨基酸可以形成一个独立的负责离子通透的孔道区模块 (Pore module),而剩余的氨基段约2200个氨基酸能够作为一个独立的机械传感模块 (mechanotransduction module) (图B)。
非常有意思的是,基于这一工作原理,他们可以人为构造出一类机械力门控离子通道。当把Piezo1蛋白的机械传感模块与正常不具备机械敏感性的酸敏感离子通道嵌合在一块,就能赋予该人造嵌合体离子通道机械力敏感性,有力佐证了他们所提出的Piezo1离子通道的工作机制模型。

研究组的研究还进一步鉴定了孔道区上决定离子通透性质(譬如单通道电导、孔道区阻断、阳离子和阴离子之间或二价阳离子与一价阳离子之间的选择性)的关键氨基酸位点(图C)。这些研究结果有力推动了我们对这一类全新的重要离子通道蛋白的离子通透和机械力传导机制的理解,也为将来以Piezo通道为靶点的药物设计与开发提供理论依据。
清华大学生命学院博士研究生赵前程、吴坤、药学院博士后耿洁和技术员池少鹏为本文并列第一作者,肖百龙研究员为本文通讯作者。此外,生命学院博士研究生王燕峰、张明敏和医学院博士研究生支鹏也参与了部分研究工作。本项目受到清华-北大生命联合中心、科技部重大研究计划、中组部青年千人计划、国家自然科学基金委优秀青年科学基金的支持。
论文链接:http://www.cell.com/neuron/fulltext/S0896-6273(16)00093-3
原创文章,如若转载,请注明出处。