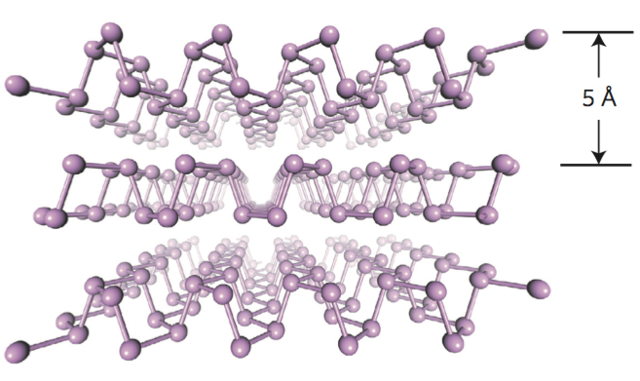
黑磷是一种有金属光泽的晶体,是磷的同素异形体中密度最大、热力学最稳定以及性质最不活泼的一种。它是高聚的不溶性固体。它是用白磷在很高压强(12000大气压)和较高温度下转化而形成的[1]。
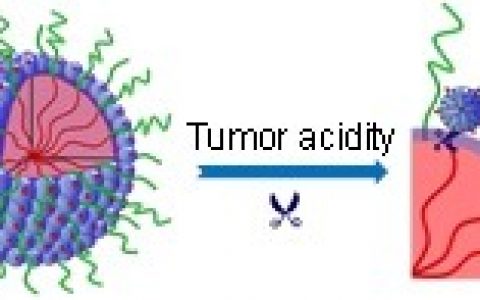
在黑磷二维材料的生物医学应用研究过程中,由深圳大学的张晗教授、清华大学的梅林副教授以及哈佛大学的施进军教授带领的联合课题组发现,黑磷纳米薄片(Nanosheets)具备优异的光学及光热转化性质、良好的生物相容性、表面易于功能化和较大的比表面积。二维黑磷纳米薄片较大的比表面积能够为化疗药物分子的大量吸附奠定基础,同时在808 nm激光照射下能够产生局部高热,一方面可以用于肿瘤的光热治疗,另一方面也能够驱动药物的释放。
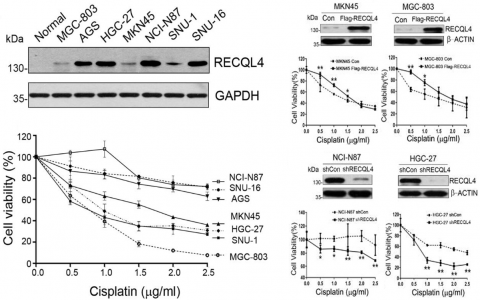
该项目研究采用优化的液态剥离法,首次将黑磷二维纳米薄片应用于诊断治疗制剂载体的制备以及功能化修饰,研发了一种负载临床化疗药物阿霉素(DOX)的黑磷纳米片载体系统,为黑磷二维材料在生物医学领域的应用提供了新思路,揭开了黑磷材料作为载药系统研究的新篇章。结果显示黑磷纳米薄片对于DOX的负载量显著高于传统的聚合物纳米粒子载体(Polymeric Nanoparticles)。同时,该项报道首次筛选并验证了黑磷纳米薄片被肿瘤细胞摄取后主要通过“大胞饮(Macropinocytosis)→晚期胞内体(Late Endosomes)→溶酶体(Lysosomes)”和“胞膜窖介导的摄取通路(Caveolae-dependent Endocytosis)”进行细胞内活动,从而为其他兴起的二维纳米材料相关细胞机制的研究提供了研究参考。该项研究还对黑磷载药纳米薄片在生物体内的安全性和抑瘤效果也进行了初步的报道,验证了黑磷载药纳米薄片具备很好的生物相容性,并且研究中采用的生物响应调节的化疗-光热治疗联合治疗(三重响应协同疗法)在免疫缺陷的裸鼠身上取得了强化的抑瘤效果。本项目的研究为黑磷在生物医学中的应用提供了新的思路,同时也为今后更为系统的动物体内研究奠定了一定的基础。
该研究获得深圳市黑磷光电技术工程实验室、美国国立卫生研究院、国家自然科学基金、深圳市孔雀团队、深圳市科创委基础布局等经费的支持。
论文链接:http://onlinelibrary.wiley.com/doi/10.1002/adma.201603276/full
[1] Wikipedia: https://en.wikipedia.org/wiki/Allotropes_of_phosphorus
(据深圳大学)
原创文章,如若转载,请注明出处。